Cómo un embrión humano comienza a formarse a partir de un par de células de sus progenitores es algo que no terminamos de comprender del todo. Sencillamente, porque no resulta admisible usar embriones viables de persona para hacer experimentos invasivos que, seguramente, terminarían en su destrucción a partir de cierto nivel de desarrollo. Por eso, desde hace unos años, ha surgido un campo de investigación no menos controvertido: el de los blastoides. Una especie de embriones sintéticos de laboratorio, que sirven de modelo de estudio de lo que seguramente ocurre en el vientre materno humano. En 2021, Nicolas Nivron consiguió emular el inicio de una gestación in vitro sin óvulo ni espermatozoide. Pero nunca un embrión implantable.
Esta vez, un equipo de investigadores de China ha ido un poco más lejos. Ha conseguido crear estructuras similares a embriones de macaco y los ha implantado en ocho hembras. Esos blastoides no han tenido una madre y padre biológicos. Han sido producto de la ingeniería genética de células madre, en placas de laboratorio. Esta tecnología es bien conocida. Pero lo novedoso es que la implantación de esos embriones sintéticos no sólo ha sido exitosa: al menos tres de las monas comenzaron a gestar. Estaban, técnicamente, preñadas. Y sin intervención de ningún macaco en la fecundación.
En un artículo publicado en la revista Cell Stem Cell, el equipo coliderado por Zhen Liu, de la Academia de Ciencias de China en Shanghái da los detalles de su trabajo con blastoides. Su obra se parece tanto a los blastocistos naturales, que han conseguido mantener su desarrollo y que las monas hayan creado sacos gestacionales tempranos.
“Esta investigación ha creado un sistema similar a un embrión artificial que puede inducirse y cultivarse indefinidamente”, ha asegurado su colega y coautor Quian Sun en la presentación. “Proporciona nuevas herramientas y perspectivas para la exploración posterior de embriones de primates y la salud médica reproductiva”.
Un paso para entender la gestación de embriones humanos sin humanos
Tres de las macacos, de la especie Cynomolgus, tuvieron una una respuesta hormonal similar al embarazo tras algo más de diez días. Eso sí, poco después, ‘abortaron‘. Realmente nunca llegó a formarse feto alguno, algo que la comunidad experta cree imposible en las condiciones en que se ha realizado el experimento.
Los investigadores comenzaron con células madre embrionarias de macacos. Las expusieron a una serie de químicos, conocidos como factores de crecimiento, en cultivo celular. Las células madre empezaron a formar estructuras similares a embriones o, más bien, blastocitos, que son los protoembriones cuando apenas han pasado cinco o seis días desde la fecundación y ya hay unas 200 células.
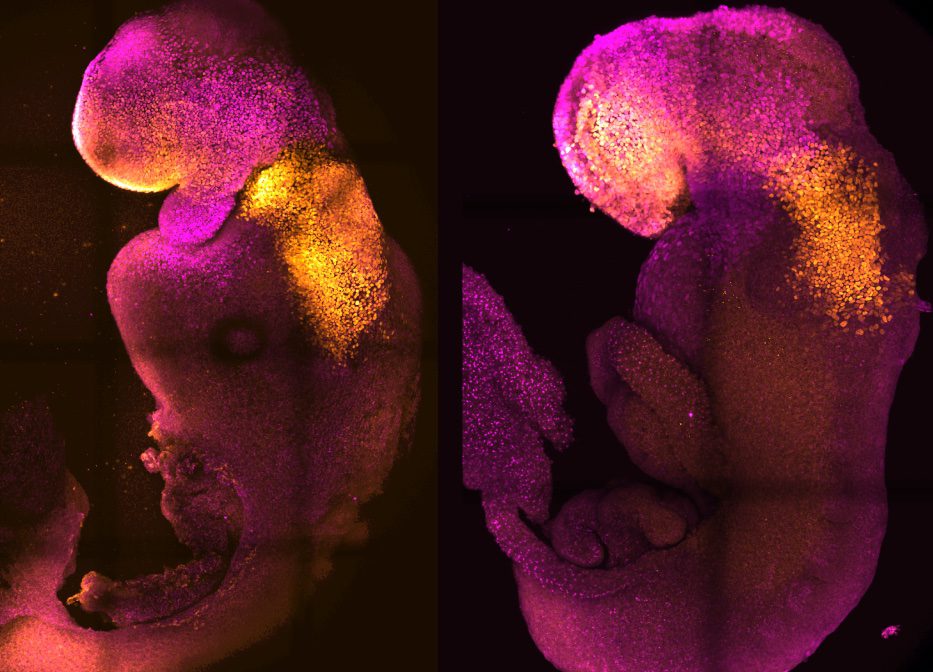
Estos bastocitos o embriones sintéticos de mono se pasaron al microscopio y no quedó duda de que su estructura era muy similar a la esperable en un proceso natural. A medida que se desarrollaron más in vitro, formaron elementos como el amnios y el saco vitelino e incluso una primitivísima vena. Los blastoides también comenzaron a formar los tipos de células que eventualmente forman las tres capas germinales.
Después hicieron una secuenciación del ARN de los diferentes titpos de célula que se habían formado, para ver que realmente eran iguales a los esperables en una gestación. En efecto, tenían patrones de expresión génica similares a las células que se encuentran en blastocistos naturales. Estaban listos para ser implantados. Y es lo que se hizo con un grupo paralelo de blastoides cultivados.
Los embriones sintéticos prosperaron sólo en 3 de 8 monas, sin formar fetos
Los blastoides o pseudo embriones sintéticos se transfirieron a los úteros de 8 monas. Al menos tres de ellas empezaron a liberar progesterona y gonadotropina coriónica, hormonas normalmente asociadas con el embarazo. Sus cuerpos interpretaron que estaban gestando una cría. Los blastoides también siguieron formando los sacos de gestación temprana, esas estructuras llenas de líquido que se desarrollan en el embarazo para contener un embrión y líquido amniótico.
Las monas ‘gestaron’ los embriones sintéticos durante una semana. Después, desaparecieron de sus cuerpos.
Hasta ahí, casi todo como en una gestación. Sin embargo, nunca llegaron a formar fetos y las estructuras desaparecieron después de aproximadamente una semana. Fin del experimento in vivo. Pero el equipo de Liu quiere ir más allá.
“Esto nos proporcionará un modelo útil para estudios futuros”, dice el coautor Fan Zhou de la Universidad de Qinghua. Los investigadores planean centrarse en desarrollar aún más el sistema de cultivo de estructuras similares a embriones a partir de células de mono. “La aplicación adicional de blastoides de mono puede ayudar a entender los mecanismos moleculares del desarrollo embrionario de los primates”. Pero no hablan de producir monos (ni, desde luego, fetos humanos) artificialmente.
Para Antonio Urries (QuirónSalud Zaragoza), presidente de la Asociación para el Estudio de la Biología de la Reproducción, “poder hacer este tipo de investigaciones en una especie tan estrechamente relacionada con la nuestra como los monos macacos supone un modelo ideal para el estudio en detalle de las primeras fases de desarrollo de órganos tan vitales de los mamíferos como son el corazón, cerebro o tubo neural. El comienzo de la organogénesis”, comenta en el SMC de España.
Estos experimentos son impensables en humanos. No se puede llevar el desarrollo de embriones atificiales más allá de dos semanas y está prohibida su implantación en útero. Los investigadores chinos reconocen las preocupaciones éticas que rodean este tipo de investigación, pero enfatizan que aún existen muchas diferencias entre estas estructuras similares a embriones y los blastocistos naturales. Es importante destacar que las estructuras similares a embriones no tienen un potencial de desarrollo completo. Señalan que para que este campo avance es importante tener discusiones entre la comunidad científica y el público.
Algo parecido ya se usa en ratones mutantes
Los avances de los últimos años con células de primates se va acercando a lo que ya es casi ‘rutina’ con roedores. Lluís Montoliu (CNB-CSIC y CIBERER-ISCIII), experto en edición genética, ratones de experimentación y bioética, recuerda que desde hace años se usan células sacadas de un blastocito natural para regenerar un ratón entero, implantándolas en otro embrión o protoembrión. “Esto ha servido para generar miles de ratones mutantes que se usan como modelos para investigar enfermedades humanas”, explica. Pero no implica que esos ratones carezcan de progenitores y sean una fabricación puramente ‘artificial’.
Las células madre embrionarias de roedor (mESC) “han servido para generar los miles de ratones mutantes existentes en la actualidad o derivar cualquier otro tipo celular in vitro, en el laboratorio”. Esto es distinto a lo presentado el año pasado en Cambridge y California, donde consiguieron algo parecido a lo hecho con los macacos: embriones de ratón sin progenitores, “con poca eficiencia”. En aquel caso, no se implantaron en ningún útero.
▸ Ingeniería genética. 2022.
Consiguen crear embriones sintéticos de ratón sin progenitores a partir de células madre
Toda esa versatilidad que muestran las células de ratones no se puede trasladar a las de los humanos. Montoliú, además de reconocer que son diferentes, no hay amparo legal ni ético para hacerlo. Sin embargo, las células de macaco ya son más cercanas a las nuestras. “Es una especie de aproximación a un experimento con humanos que actualmente sería irrealizable”, explica el doctor.
“Cada vez estamos más cerca de ver el nacimiento de primates no humanos íntegramente derivados de células troncales pluripotentes embrionarias cultivadas en el laboratorio”. Es decir, conseguir monos sin óvulos ni espermatozoides implicados, “como ya es posible en ratones”.
Cada vez estamos más cerca de ver el nacimiento de primates no humanos íntegramente derivados de células cultivadas en el laboratorio
Lluís Montoliu, CNB-CSIC
Alfonso Martínez Arias (ICREA) e investigador en Sistemas de Bioingeniería-MELIS de la Universidad Pompeu Fabra, también expresa en el SMC de España la importancia del paso dado por el equipo chino. Han demostrado que han “producido las semillas de cada tejido y órgano”. Pero, además, en un útero, no en condiciones de laboratorio. “Hasta ahora no había evidencia de que los blastoides pudieran implantarse correctamente e iniciar el desarrollo del embrión”.
Eso sí, le parece un trabajo todavía muy alejado de la posibilidad de que salga adelante un embrión viable. “Mi impresión es que el proceso de gastrulación es defectuoso. Los pocos embriones que inician esta fase crucial del desarrollo colapsan al poco de iniciar el proceso”.
Los macacos y los humanos, cercanos evolutivamente, son también diferentes, “incluso en la manera en la que los blastocistos implantan”. De ahí que, por el momento, este tipo de experimentos estén muy lejos de algo que es total ficción y poca ciencia: crear bebés sin fecundación de óvulo alguno.
- Estudio de Li et al. en ‘Cell Steam Cell’, 2023
- Estudio con los primeros blastoides de Kagawa y Rivron en ‘Nature’, 2021
- Zhen Liu (Academia China de Ciencias)
- Antonio Urries (AEBR)
- Lluís Montoliu (CNB-CSIC)
- Alfonso Martínez Arias (ICREA, UPF)




