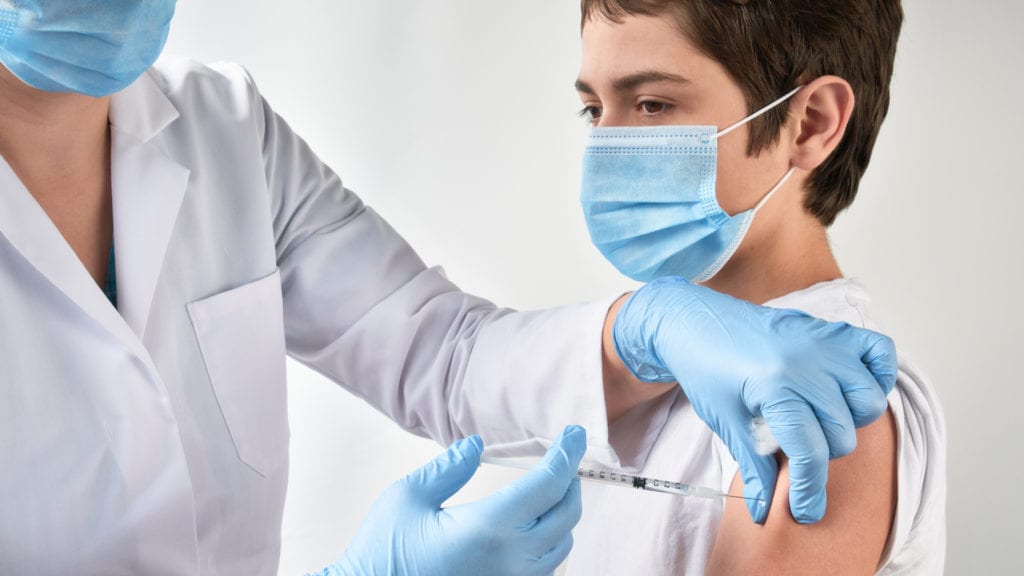
Canadá se ha convertido esta semana en el primer país en autorizar la vacuna contra la COVID-19 de Pfizer-BioNtech en niños a partir de los 12 años. El Ministerio de Sanidad del país lo anunció el pasado 5 de mayo tras comprobar que la vacuna es “segura y eficaz” en ese grupo poblacional.
Solo dos días antes, la Agencia Europea del Medicamento (EMA) inició la evaluación de los nuevos estudios sobre esta vacuna para decidir si incluye a los jóvenes de 12 a 15 años en el programa de vacunación de la Unión Europea. ¿Para cuándo se espera la decisión de la EMA? ¿Qué datos tienen en cuenta las agencias reguladoras para garantizar la seguridad de la vacuna en niños? Te lo explicamos.
Canadá autoriza el uso de la vacuna de Pfizer en los jóvenes tras comprobar que es “segura”
“Un hito importante en la lucha de Canadá contra la pandemia de COVID-19”. Con estas palabras presentó el Ministerio de Sanidad canadiense su decisión de autorizar la vacuna de Pfizer-BioNtech en las personas de entre 12 y 15 años. Hasta el momento solo se podía vacunar en el país a los jóvenes de 16 años o más.
Según explica el Gobierno canadiense en un comunicado, antes de extender la autorización de uso de la vacuna de Pfizer-BioNtech, se realizó una «revisión científica rigurosa e independiente de la evidencia conocida».
En concreto, las autoridades canadienses estudiaron los datos de un ensayo clínico (prueba de investigación de la vacuna en personas) de la vacuna de Pfizer-BioNtech en el que participaron 2.260 voluntarios de 12 a 15 años de edad en los Estados Unidos.
Estos estudios en niños y adolescentes se realizan cuando ya hay datos que avalan la seguridad de esa vacuna en otros cohortes de edad. El seguimiento de la seguridad de estos ensayos en menores “es enorme y está totalmente garantizado”, insiste a Newtral.es el virólogo del Centro de Superior de Investigaciones Científicas (CSIC) Mariano Esteban.
“Además los ensayos son progresivos: se empieza con un número reducido de personas y se va ampliando poco a poco el número de participantes para controlar la posible aparición de efectos adversos”, precisa Esteban.
En cualquier caso, el Ejecutivo de Canadá ha destacado que continuará vigilando la seguridad de la vacuna y reclamará a Pfizer-BioNTech información constante “sobre la seguridad, eficacia y calidad de la vacuna en este grupo de edad” para “garantizar que sus beneficios continúan una vez que esté en el mercado”.
La Unión Europea estudia si autorizar la vacunación contra la COVID-19 en jóvenes a partir de 12 años
Se espera que Estados Unidos siga los pasos de su país vecino y de luz verde al uso de la vacuna para ese rango de edad en los próximos días, según recoge el medio estadounidense The New York Times.
La Agencia Europea del Medicamento (EMA, por sus siglas en inglés) también comenzó el pasado 3 de mayo a evaluar los datos presentados por Pfizer y BioNtech sobre sus estudios de la vacuna en niños y adolescentes.Este organismo europeo prevé tener en junio su veredicto.
Por ahora, el Ministerio de Sanidad español recuerda que “la población infantil y adolescente de hasta 16 años no se ha considerado como un grupo prioritario a vacunar, ya que existen otros grupos de población con mayor riesgo de enfermedad grave y complicaciones”.
También se espera que otras farmacéuticas como Moderna o Janssen, que también están realizando ensayos clínicos autorizados con menores de edad, algunos de ellos en España, soliciten a la EMA la autorización de sus vacunas en ese grupo poblacional cuando tengan listos sus resultados.
La importancia de vacunar a los niños
Como ya contamos en Newtral.es, la mayoría de estudios coinciden en que los niños desarrollan menos síntomas y los que los tienen son menos graves que en los adultos. Pero eso no implica necesariamente que tengan menor poder de transmisión del virus.
Es necesario que la población pediátrica también se vacune “con el fin de conseguir la ansiada inmunidad de rebaño”, insiste a Newtral.es el coordinador de ensayos clínicos en el Hospital La Paz de Madrid Alberto Borobia.
El médico recuerda que habrá población adulta que no podrá vacunarse, debido a ciertas patologías y comorbilidades, por tanto, “es importante que todo el entorno de estas personas, incluidos los niños, esté vacunado. Es una manera de protegerlos”.
Fuentes:
-Artículo de The New York Times sobre cuándo planea la FDA aprobar la vacunación contra la COVID-19 en personas a partir de 12 años.
-Coordinador de ensayos clínicos en el Hospital La Paz de Madrid Alberto Borobia.
–Comunicado de la EMA sobre la revisión de los datos de los ensayos clínicos de Pfizer en menores.
–Comunicado de Pfizer con los resultados de sus ensayos clínicos en menores.
-El virólogo del Centro de Superior de Investigaciones Científicas (CSIC) Mariano Esteban